为确保药品安全、有效和质量可控,国家对批准上市的药品实行再注册制度。本文将系统梳理陕西省国产药品再注册审批的关键信息,包括申请条件、收费标准、材料清单、办理流程,并介绍相关的代理与缴费服务,为相关企业提供实用参考。
一、 申请条件
根据《药品注册管理办法》,申请国产药品再注册,药品批准文号持有人(以下简称“持有人”)需满足以下基本条件:
- 文号有效:持有的药品批准文号在有效期内(通常为5年)。
- 符合法规:药品生产符合《药品生产质量管理规范》(GMP)要求。
- 持续合规:在药品批准文号有效期内,该药品生产、销售、不良反应监测等情况符合国家相关规定,未出现严重质量问题或安全隐患。
- 资料完整:能够按照要求提交完整的再注册申请资料。
- 其他要求:符合国家药品监督管理局及陕西省药品监督管理局规定的其他条件。
二、 收费标准及依据
目前,国产药品再注册审批不收取官方的审批费用。
依据:根据国家发展改革委、财政部关于药品、医疗器械产品注册收费标准的相关通知,国产药品再注册暂未设立收费项目。但申请人需自行承担资料准备、检验检测(如需要)、第三方服务等相关成本。
三、 申请材料清单
申请人需向陕西省药品监督管理局提交以下材料(具体要求以最新官方指南为准):
- 《药品再注册申请表》:通过国家药品监督管理局网上办事大厅在线填报并打印。
- 证明性文件:
- 药品批准证明文件及其附件的复印件(包括药品注册批件、补充申请批件、药品标准等)。
- 药品生产许可证及其变更记录页复印件。
- 《药品生产质量管理规范》认证证书复印件。
- 营业执照复印件。
- 五年内生产、销售、抽验、不良反应监测情况报告:详细说明药品的生产批次、销售数量、质量抽检结果、不良反应收集与处理情况等。
- 五年内药品制剂变更情况报告:汇总并说明所有已批准的变更(如工艺、场地、质量标准等)。
- 药品处方、生产工艺、质量标准、药品说明书和标签样稿:需与现行批准内容一致,如有变更应已获批。
- 生产药品制剂所用原料药的批准证明文件(如为制剂)。
- 药品最小销售单元的包装、标签和说明书实样。
- 申请人对其申请材料真实性负责的承诺书。
- 省局要求的其他资料。
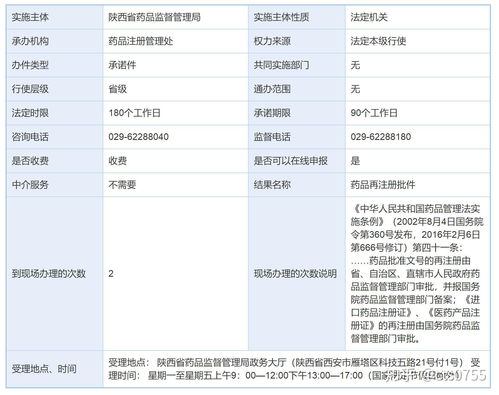
四、 办理流程
- 网上填报:登录“国家药品监督管理局网上办事大厅”,在线填写并提交《药品再注册申请表》。
- 材料准备与自查:根据清单准备全套纸质申请材料,并确保内容真实、完整、规范。
- 提交申请:将纸质申请材料报送至陕西省药品监督管理局受理大厅(或通过邮寄方式)。
- 受理审查:省局对材料进行形式审查,符合要求的予以受理,出具受理通知书;不符合要求的,一次性告知需要补正的内容。
- 技术审评与审批:省局组织对申请材料进行技术审评,必要时进行现场检查或抽样检验。审评通过后,作出予以再注册或不予再注册的审批决定。
- 领取批件:审批通过后,持有人凭受理通知书及相应凭证领取《药品再注册批件》。
总办理时限:通常为120个工作日(不含申请人补正材料的时间)。
五、 干货分享:代理办理辅导与缴费服务
对于不熟悉流程、人力紧张或希望提高效率的企业,可以寻求专业的第三方服务。
- 代理办理辅导服务:
- 服务内容:专业机构提供从政策解读、申请方案制定、资料撰写与审核、申报系统操作指导到进度跟踪、沟通协调等全流程或关键环节的辅导与代理服务。
- 价值:帮助企业规避常见错误,确保材料质量,节省时间成本,提升申报成功率。
- 选择建议:选择在陕西本地有丰富药品注册经验、信誉良好的咨询公司或律师事务所,并确认其服务团队的专业资质。
- 本地及异地代缴费服务:
- 服务说明:虽然再注册本身无官方收费,但在药品生命周期中,企业可能涉及其他相关规费(如药品补充申请费、检验费等)。一些代理机构或金融服务平台可提供便捷的代缴服务。
- 本地服务:通常由本地代理机构直接代为处理向省内相关部门缴纳的费用。
- 异地服务:主要针对持有人所在地与陕西省外,需要向国家局或外省机构缴费的情况,通过委托代理进行跨区域支付,解决异地奔波问题。
- 注意事项:选择代缴费服务时,务必核实服务提供方的正规性与安全性,明确费用明细和服务协议,保障资金安全。
****:陕西国产药品再注册是一项法规性、专业性强的常态化工作。持有人应提前规划,严格对照条件与清单准备,亦可借助专业服务确保流程顺畅,从而保障药品批准文号的持续有效性,保障企业正常生产经营。